
|
시장보고서
상품코드
1836480
등온 핵산 증폭 기술(INAAT) : 시장 점유율 분석, 산업 동향, 통계, 성장 예측(2025-2030년)Isothermal Nucleic Acid Amplification Technology - Market Share Analysis, Industry Trends & Statistics, Growth Forecasts (2025 - 2030) |
||||||
 Mordor Intelligence
Mordor Intelligence
등온 핵산 증폭 기술(INAAT) 시장 규모는 2025년에 53억 6,000만 달러에 달하고, 예측 기간(2025-2030년)의 CAGR은 8.87%를 나타내, 2030년에는 81억 9,000만 달러에 달할 것으로 전망됩니다.
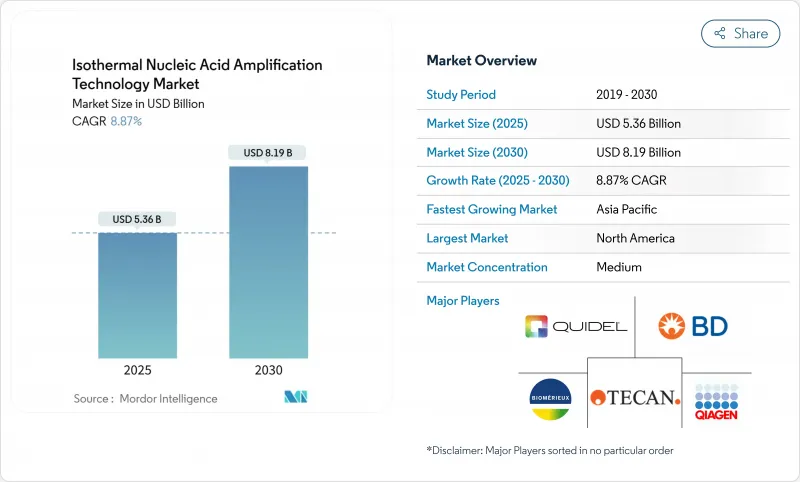
성장을 뒷받침하는 것은 부피가 큰 열 순환기의 필요성을 없애고 신속한 요점 검사를 지원하는 항온 증폭입니다. 병원은 INAAT 플랫폼을 긴급 검사 장치에 도입하여 검사 결과를 몇 시간에서 몇 분으로 단축하고 시약 공급업체는 안정적이고 이익률이 높은 소모품 판매로부터 이익을 얻고 있습니다. 제조업체 각사는 마이크로플루이딕스, 동결건조 시약, 비색 검출을 통합하여 검사 1건당 비용을 낮추고 검사실 이외의 환경에서의 사용을 확대하고 있습니다. 아시아태평양에서는 장비 승인의 합리화로 시장 출시까지의 시간이 단축되므로 채택이 가속화되고 있습니다. 한편, 북미에서는 상환의 틀이 확립되어 있기 때문에 매출에서 리드하고 있습니다.
세계의 등온 핵산 증폭 기술(INAAT) 시장 동향과 인사이트
POC(Point-of-Care) 감염증에의 채용
응급 부서는 현재 INAAT 호흡기 패널에 의존하고 있습니다. INAAT는 실험실 수준의 답변을 몇 분 안에 제공하여 환자의 처리 능력과 항생제 스튜어드십을 향상시킵니다. 세파이드사의 Xpert HCV가 2024년 6월에 FDA로부터 인가되어, 손가락 끝의 혈액 샘플로부터 당일 C형 간염 진단이 가능하게 되었습니다. 결과 정밀도는 PCR 방법과 동등하며, 정온 반응은 제한된 자원 환경에서 유용한 배터리 구동 휴대용 기기에 적합합니다.
고령화와 만성질환 부담
65세 이상의 인구에서는 감염과 암의 재발에 대한 정기적인 바이오마커 검사가 필요합니다. INAAT 기반의 리퀴드 바이옵시 시스템은 94.1%의 감도로 미세 잔류 병변을 검출할 수 있어 집이나 지역의 클리닉에서의 모니터링이 가능합니다. 원격 의료 플랫폼과의 통합은 결과 검토를 간소화하고 불필요한 병원 진찰을 억제하고 시스템 비용을 절감합니다.
PCR 및 DCR 플랫폼과의 경쟁
확립된 PCR 인프라는 기존의 증폭 워크플로우에 최적화된 열 사이클링 플랫폼, 자동 샘플 처리 시스템, 기술자 교육 프로그램에 투자해 온 실험실에 있어서 큰 전환 비용이 됩니다. 디지털 PCR 플랫폼은 특히 정확한 바이러스량 모니터링 및 복사 수의 변동 분석을 필요로 하는 용도에서 INAAT가 현재 대응할 수 없는 절대 정량 능력을 제공함으로써 경쟁을 더욱 격화시키고 있습니다. 검사 시설의 책임자는 INAAT의 채용을 평가할 때 기존의 품질 관리 절차, 규제의 타당성 확인, 직원의 능력이 PCR 방법과 일치하기 때문에 워크플로우가 혼란될 우려가 있습니다.
보고서에서 분석된 기타 성장 촉진요인 및 억제요인
- PCR법에서 INAAT법으로의 워크플로우의 이행
- 검사 1건당 비용 저감 경제성
- 인식과 상환의 격차
부문 분석
LAMP는 2024년에 등온 핵산 증폭 기술(INAAT) 시장의 44.34%를 차지했고 2030년까지 13.36%의 연평균 복합 성장률(CAGR)을 나타낼 것으로 예측되고 있습니다. 이 기술은 6개의 유전자 영역을 표적으로 하며, 열 사이클링 없이 높은 특이성을 제공합니다. HDA 및 NEAR와 같은 보완적인 접근법은 저온 이용 사례에 대응하고, TMA는 RNA 검출이 중요한 혈액 스크리닝으로 가치를 유지합니다.
LAMP와 CRISPR-Cas 시스템의 조합을 통해 30분 안에 아토몰 감도를 달성할 수 있게 되었으며, 검출 기술 혁신이 등온 핵산 증폭 기술(INAAT) 시장을 재구성하고 있습니다. 비색 래터럴 플로우 스트립은 카트리지에 직접 통합되어 형광 리더가 없는 클리닉에서의 채용이 넓어지고 있습니다.
시약 및 소모품은 2024년 매출의 63.56%를 차지하며 연구 개발을 지원하는 경상 현금 흐름을 제공했습니다. Bst 폴리머라제는 대부분의 INAAT 키트를 지원하므로 공급 안정성은 여전히 중요합니다. 이 장비는 iPonatic의 30분 카트리지가 워크플로를 완전히 자동화할 수 있도록 공급업체가 마이크로플루이딕스와 원스텝 추출을 통합하여 연간 11.24% 증가합니다.
이 장비의 혁신은 통합과 소형화에 중점을 두고 있으며, 제조업체는 단일 샘플 카트리지 형식으로 샘플 준비, 증폭 및 검출을 결합한 휴대용 플랫폼을 개발하고 있습니다. iPonatic 시스템은 이러한 추세를 보여주며 실온 추출과 통합 검출 기능을 사용하여 30분 이내에 완전한 핵산 검사를 실현합니다. 마이크로유체의 통합은 시약 소비와 오염 위험을 줄이면서 정확한 유체 취급과 온도 제어를 가능하게 하지만, 제조의 복잡성과 비용을 고려하여 고가치의 응용 분야를 채택하는 데 한계가 있습니다.
등온 핵산 증폭 기술(INAAT) 시장 보고서는 기술별(Helicase-Dependent Amplification(HDA), 기타), 제품별(장치, 기타), 용도별(감염증 진단, 기타), 최종 사용자별(병원, 레퍼런스 랩, 기타), 지역별(북미, 유럽, 아시아태평양, 기타)에 업계를 세분화하고 있습니다. 시장 예측은 금액(달러)으로 제공됩니다.
지역별 분석
북미는 2024년 35.67%의 매출로 선도했으며, 15분의 호흡기 패널을 클리닉에 도입하는 CLIA 면제규칙 등 FDA 경로에 뒷받침되는 광범위한 보험 적용으로 병원은 예산을 중단하지 않고 INAAT를 채용할 수 있습니다. 연구자금과 왕성한 벤처캐피탈이 국내기기 발매를 가속시킵니다.
아시아태평양은 성장 엔진이며 CAGR 15.64%를 나타낼 것으로 예측됩니다. 중국의 NMPA는 심사기간을 24개월에서 12개월로 단축해 다국적 기업의 현지 생산을 유치 nmpa.gov.cn. 일본의 노인 인구는 재택진단에 박차를 가하고 인도의 공중보건 프로그램은 결핵과 뎅기열 감시용으로 저렴한 INAAT 키트를 조달하고 있습니다. 현지 생산은 외환 위험을 줄이고 세계적인 혼란시에도 공급을 보장합니다.
유럽에서는 IVDR에 의한 규격의 조화가 진행되고 꾸준히 성장하고 있지만, 소규모의 혁신적 기업은 CE 마킹을 위한 근거의 허들이 높습니다. 독일과 영국은 강력한 병원 네트워크와 트랜스레이셔널 리서치의 결과로 수요를 지원하고 있습니다. 비용 억제 정책은 PCR에 비해 에너지와 노력을 절약할 수 있는 항온 시스템을 지원합니다.
기타 혜택 :
- 엑셀 형식 시장 예측(ME) 시트
- 3개월의 애널리스트 서포트
목차
제1장 도입
- 조사 전제조건과 시장 정의
- 조사 범위
제2장 조사 방법
제3장 주요 요약
제4장 시장 상황
- 시장 개요
- 시장 성장 촉진요인
- POC(Point-of-Care) 감염증의 보급
- 고령화와 만성질환 부담
- PCR에서 INAAT로 워크플로우 이동
- 검사 1건당 비용 절감
- 마이크로플루이딕스 배터리 구동 카트리지(UTR)
- Crispr로 강화된 분석의 특이성(UTR)
- 시장 성장 억제요인
- PCR 및 DCR 플랫폼과의 경쟁
- 인식과 상환의 갭
- Bst 시약의 효소 공급의 불안정성
- 엄격한 CLIA 면제/IVDR 근거의 장애물(UTR)
- Porter's Five Forces 분석
- 신규 참가업체의 위협
- 구매자의 협상력
- 공급기업의 협상력
- 대체품의 위협
- 경쟁 기업 간 경쟁 관계
제5장 시장 규모·성장 예측
- 기술별
- 헬리카제 의존 증폭(HDA)
- 니킹 효소 증폭 반응(NEAR)
- 루프 매개 등온 증폭(LAMP)
- 가닥 치환 증폭(SDA)
- 핵산 서열 기반 증폭(NASBA)
- 전사 매개 증폭(TMA)
- 단일 프라이머 등온 증폭(SPIA)
- 기타 기술
- 제품별
- 장비
- 시약 및 소모품
- 용도별
- 감염성 질환 진단
- 종양학 및 액체 생검
- 혈액 검사 및 수혈 안전성
- 식품 및 수질 안전성 검사
- 수의사 및 농업 진단
- 최종 사용자별
- 병원 및 레퍼런스 랩
- POC(Point-of-Care)/분산형 진료소
- 학술 및 연구 기관
- 지역별
- 북미
- 미국
- 캐나다
- 멕시코
- 유럽
- 독일
- 영국
- 프랑스
- 이탈리아
- 스페인
- 기타 유럽
- 아시아태평양
- 중국
- 일본
- 인도
- 호주
- 한국
- 기타 아시아태평양
- 중동 및 아프리카
- GCC
- 남아프리카
- 기타 중동 및 아프리카
- 남미
- 브라질
- 아르헨티나
- 기타 남미
- 북미
제6장 경쟁 구도
- 시장 집중도
- 시장 점유율 분석
- 기업 프로파일
- Abbott Laboratories
- Amplifica Labs
- Becton, Dickinson & Co.
- BioMerieux SA
- DiaSorin SpA
- Eiken Chemical Co., Ltd.
- Genomera Inc.
- Hologic Inc.
- Lucigen(LGC Biosearch)
- Meridian Bioscience
- Molbio Diagnostics
- New England Biolabs
- OptiGene Ltd.
- Qiagen NV
- QuidelOrtho Corp.
- Roche Diagnostics
- Tecan Genomics Inc.
- Thermo Fisher Scientific
- TwistDx Ltd.
- Ustar Biotechnologies
제7장 시장 기회와 전망
KTH 25.10.27The Isothermal Nucleic Acid Amplification Technology Market size is estimated at USD 5.36 billion in 2025, and is expected to reach USD 8.19 billion by 2030, at a CAGR of 8.87% during the forecast period (2025-2030).
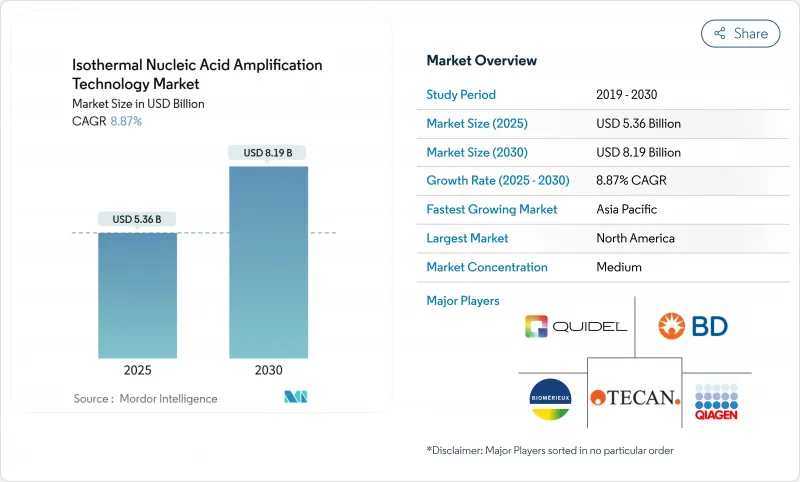
Growth is fuelled by constant-temperature amplification, which removes the need for bulky thermal cyclers and supports rapid point-of-care testing. Hospitals deploy INAAT platforms in emergency units to cut result turnaround from hours to minutes, while reagent suppliers benefit from steady, high-margin consumable sales. Manufacturers are integrating microfluidics, lyophilised reagents and colourimetric detection that lower per-test costs and broaden use in non-laboratory settings. Asia-Pacific adoption accelerates as streamlined device approvals shorten time-to-market, whereas North America leads on revenue owing to established reimbursement frameworks.
Global Isothermal Nucleic Acid Amplification Technology Market Trends and Insights
Point-of-care infectious-disease adoption
Emergency departments now rely on INAAT respiratory panels that deliver lab-quality answers in minutes, boosting patient throughput and antibiotic stewardship. FDA clearance of Cepheid's Xpert HCV in June 2024 allows same-visit hepatitis C diagnosis from a fingertip blood sample, a milestone that removes multi-visit loss to follow-up. Result accuracy remains on par with PCR while constant-temperature reactions suit battery-powered, portable devices useful in resource-limited settings.
Aging population & chronic-disease burden
Populations over 65 years demand regular biomarker checks for infections and cancer recurrence. INAAT-based liquid-biopsy systems can detect minimal residual disease with 94.1% sensitivity, enabling home or community clinic monitoring. Integration with telemedicine platforms streamlines result review, curbing unnecessary hospital visits and lowering system costs.
Competition From PCR & DCR Platforms
Established PCR infrastructure represents significant switching costs for laboratories that have invested in thermal cycling platforms, automated sample handling systems, and technician training programs optimized for traditional amplification workflows. Digital PCR platforms further intensify competition by offering absolute quantification capabilities that INAAT currently cannot match, particularly in applications requiring precise viral load monitoring or copy number variation analysis. Laboratory directors cite workflow disruption concerns when evaluating INAAT adoption, as existing quality control procedures, regulatory validations, and staff competencies align with PCR methodologies.
Other drivers and restraints analyzed in the detailed report include:
- Workflow shift from PCR to INAAT
- Lower per-test cost economics
- Awareness and Reimbursement Gaps
For complete list of drivers and restraints, kindly check the Table Of Contents.
Segment Analysis
LAMP captured 44.34% of the Isothermal Nucleic Acid Amplification Technology market in 2024 and is forecast to grow at 13.36% CAGR to 2030. The methodology targets six gene regions, conferring high specificity without thermal cycling. Complementary approaches like HDA and NEAR address low-temperature use cases, while TMA retains value in blood screening where RNA detection matters.
Detection innovation is reshaping the Isothermal Nucleic Acid Amplification Technology market as developers pair LAMP with CRISPR-Cas systems to reach attomolar sensitivity in 30 minutes. Colourimetric lateral-flow strips integrate directly into cartridges, widening adoption in clinics lacking fluorescence readers.
Reagents and consumables generated 63.56% of 2024 revenue, providing recurring cash flow that subsidises R&D. Bst polymerase supply resilience remains critical because it underpins most INAAT kits. Instruments are set to expand 11.24% annually as vendors embed microfluidics and one-step extraction, evidenced by iPonatic's 30-minute cartridge achieving full workflow automation.
Instrument innovation focuses on integration and miniaturization, with manufacturers developing portable platforms that combine sample preparation, amplification, and detection in single-use cartridge formats. The iPonatic system exemplifies this trend, delivering complete nucleic acid testing within 30 minutes using room-temperature extraction and integrated detection capabilities. Microfluidic integration enables precise fluid handling and thermal control while reducing reagent consumption and contamination risks, though manufacturing complexity and cost considerations limit adoption to high-value applications.
The Isothermal Nucleic Acid Amplification Technology (INAAT) Market Report Segments the Industry Into by Technology (Helicase-Dependent Amplification (HDA), and More), Product (Instruments, and More), Application (Infectious-Disease Diagnostics, and More), End-User (Hospitals and Reference Labs, and More), and Geography (North America, Europe, Asia-Pacific, and More). The Market Forecasts are Provided in Terms of Value (USD).
Geography Analysis
North America leads with 35.67% revenue in 2024, underpinned by FDA pathways such as CLIA waiver rules that bring fifteen-minute respiratory panels into clinics fda.gov. Extensive insurance coverage permits hospitals to adopt INAAT without budget disruption. Research funding and robust venture capital accelerate domestic device launches.
Asia-Pacific is the growth engine, forecast at 15.64% CAGR. China's NMPA shortened review timelines from 24 to 12 months, attracting multinationals to localise production nmpa.gov.cn. Japan's senior population spurs home-based diagnostics, while India's public-health programmes source affordable INAAT kits for tuberculosis and dengue surveillance. Local manufacturing dampens currency risk and secures supply during global disruptions.
Europe grows steadily as the IVDR harmonises standards, though smaller innovators face higher evidence hurdles for CE marking. Germany and the United Kingdom anchor demand through strong hospital networks and translational research output. Cost-containment policies favour constant-temperature systems that save energy and labour compared with PCR.
- Abbott Laboratories
- Amplifica Labs
- Beckton Dickinson
- bioMerieux
- DiaSorin
- Eiken Chemical Co., Ltd.
- Genomera Inc.
- Hologic
- Lucigen (LGC Biosearch)
- Meridian Bioscience
- Molbio Diagnostics
- New England Biolabs
- OptiGene Ltd.
- QIAGEN
- QuidelOrtho Corp.
- Roche
- Tecan Group
- Thermo Fisher Scientific
- TwistDx Ltd.
- Ustar Biotechnologies
Additional Benefits:
- The market estimate (ME) sheet in Excel format
- 3 months of analyst support
TABLE OF CONTENTS
1 Introduction
- 1.1 Study Assumptions & Market Definition
- 1.2 Scope of the Study
2 Research Methodology
3 Executive Summary
4 Market Landscape
- 4.1 Market Overview
- 4.2 Market Drivers
- 4.2.1 Point-of-Care Infectious-Disease Adoption
- 4.2.2 Aging Population and Chronic-Disease Burden
- 4.2.3 Workflow Shift from PCR to INAAT
- 4.2.4 Lower Per-Test Cost Economics
- 4.2.5 Microfluidic Battery-Powered Cartridges (UTR)
- 4.2.6 Crispr-Enhanced Assay Specificity (UTR)
- 4.3 Market Restraints
- 4.3.1 Competition From PCR and DCR Platforms
- 4.3.2 Awareness and Reimbursement Gaps
- 4.3.3 Enzyme-Supply Volatility for Bst Reagents
- 4.3.4 Stringent CLIA-Waiver / IVDR Evidence Hurdles (UTR)
- 4.4 Porter's Five Forces Analysis
- 4.4.1 Threat of New Entrants
- 4.4.2 Bargaining Power of Buyers
- 4.4.3 Bargaining Power of Suppliers
- 4.4.4 Threat of Substitutes
- 4.4.5 Competitive Rivalry
5 Market Size & Growth Forecasts (Value in USD)
- 5.1 By Technology
- 5.1.1 Helicase-Dependent Amplification (HDA)
- 5.1.2 Nicking Enzyme Amplification Reaction (NEAR)
- 5.1.3 Loop-Mediated Isothermal Amplification (LAMP)
- 5.1.4 Strand Displacement Amplification (SDA)
- 5.1.5 Nucleic Acid Sequence-Based Amplification (NASBA)
- 5.1.6 Transcription-Mediated Amplification (TMA)
- 5.1.7 Single-Primer Isothermal Amplification (SPIA)
- 5.1.8 Other Technologies
- 5.2 By Product
- 5.2.1 Instruments
- 5.2.2 Reagents & Consumables
- 5.3 By Application
- 5.3.1 Infectious-Disease Diagnostics
- 5.3.2 Oncology and Liquid Biopsy
- 5.3.3 Blood-Screening and Transfusion Safety
- 5.3.4 Food- & Water-Safety Testing
- 5.3.5 Veterinary and Agricultural Diagnostics
- 5.4 By End-User
- 5.4.1 Hospitals & Reference Labs
- 5.4.2 Point-of-Care / Decentralised Clinics
- 5.4.3 Academic & Research Institutes
- 5.5 By Geography
- 5.5.1 North America
- 5.5.1.1 United States
- 5.5.1.2 Canada
- 5.5.1.3 Mexico
- 5.5.2 Europe
- 5.5.2.1 Germany
- 5.5.2.2 United Kingdom
- 5.5.2.3 France
- 5.5.2.4 Italy
- 5.5.2.5 Spain
- 5.5.2.6 Rest of Europe
- 5.5.3 Asia-Pacific
- 5.5.3.1 China
- 5.5.3.2 Japan
- 5.5.3.3 India
- 5.5.3.4 Australia
- 5.5.3.5 South Korea
- 5.5.3.6 Rest of Asia-Pacific
- 5.5.4 Middle East & Africa
- 5.5.4.1 GCC
- 5.5.4.2 South Africa
- 5.5.4.3 Rest of Middle East & Africa
- 5.5.5 South America
- 5.5.5.1 Brazil
- 5.5.5.2 Argentina
- 5.5.5.3 Rest of South America
- 5.5.1 North America
6 Competitive Landscape
- 6.1 Market Concentration
- 6.2 Market Share Analysis
- 6.3 Company Profiles (includes Global level Overview, Market level overview, Core Segments, Financials as available, Strategic Information, Market Rank/Share for key companies, Products & Services, and Recent Developments)
- 6.3.1 Abbott Laboratories
- 6.3.2 Amplifica Labs
- 6.3.3 Becton, Dickinson & Co.
- 6.3.4 BioMerieux SA
- 6.3.5 DiaSorin SpA
- 6.3.6 Eiken Chemical Co., Ltd.
- 6.3.7 Genomera Inc.
- 6.3.8 Hologic Inc.
- 6.3.9 Lucigen (LGC Biosearch)
- 6.3.10 Meridian Bioscience
- 6.3.11 Molbio Diagnostics
- 6.3.12 New England Biolabs
- 6.3.13 OptiGene Ltd.
- 6.3.14 Qiagen N.V.
- 6.3.15 QuidelOrtho Corp.
- 6.3.16 Roche Diagnostics
- 6.3.17 Tecan Genomics Inc.
- 6.3.18 Thermo Fisher Scientific
- 6.3.19 TwistDx Ltd.
- 6.3.20 Ustar Biotechnologies
7 Market Opportunities & Future Outlook
- 7.1 White-Space & Unmet-Need Assessment
